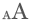Újabb magyar siker
A magazin címlapján látható képen egy enzim éppen kapcsolatot alakít ki partnereivel.
Feltárják azoknak a fehérjéknek a szerkezetét és működését, amelyek a környezetből érkező ingerek fogadásában, sejten belüli feldolgozásában és a biológiai válasz kiváltásában játszanak szerepet – foglalta össze kutatásaik lényegét az MTI kérdésére Reményi Attila, az ELTE Biokémiai Tanszékén tevékenykedő kutatócsoport vezetője annak kapcsán, hogy munkájuk eredményét címlapon hozta a Science Signaling című rangos tudományos magazin legfrissebb száma.
Az általuk is vizsgált receptormolekulák jelentőségét mutatja, hogy az idei kémiai Nobel-díjat is ez a terület kapta. A díjazott amerikai kutatók munkája révén megnyílt az út olyan hatóanyagok tervezése felé, amelyek segítségével a korábbinál lényegesen hatékonyabban és pontosabban lehet a receptorokat ki- és bekapcsolni.
Reményi Attila kutatócsoportja a receptorfehérjék bekapcsolása utáni, a folyamatban későbbi lépésekkel foglalkozik. „Az ingerek hatására a sejtmembránon aktiválódó receptorok után egy többlépcsős, sejten belüli fehérjekaszkád lép működésbe. E kaszkád fontos összetevőivel, a jelpályák köztes enzimjeivel dolgoztunk, amelyek a sejtes válaszok sokszínűségéért felelősek. Ezek az enzimek szerepükből adódóan sokféle fehérjével alakítanak ki fizikai kapcsolatot” – magyarázta a kutatásvezető.
A csoport ötéves kutatómunkával tárta fel azt a molekuláris felszínt, amelynek révén a szóban forgó fehérjék kölcsönható partnereikhez kötődnek. Az áttörés egy szerkezeti biokémiai megközelítésnek köszönhető, amellyel a Reményi-labor meghatározta négy különböző molekula szerkezetét: az enzimet abban a pillanatban fényképezték le, amikor az éppen kapcsolatot alakít ki partnereivel.
„A magazin címlapján látható kép három fehérjét ábrázol, más színnel mutatva a kölcsönható fehérjékből származó molekularészletet. Alapvetően fontos, hogy az egyes atomok pontosan milyen szerepet töltenek be a kapcsolódásnál” – fejtette ki Reményi.
A kutató utalt rá, hogy a jelátadásban bekövetkezett hibák vezetnek el végső soron a különböző krónikus betegségekhez. A csoport a jövőben azt tervezi, hogy az így feltárt háromdimenziós molekuláris térkép segítségével a korábbiaknál sokkal specifikusabban működő hatóanyagokat hoz létre, amelyek segítségével a rák és különböző gyulladásos folyamatokhoz köthető betegségek lesznek kezelhetők.
A külföldről tíz év után öt éve hazatért laborvezető a Fehérje-Fehérje Interakció Kutatócsoportot az ELTE Biokémiai Tanszékén magyar és külföldi pályázatok támogatásával hozta létre. A kísérleti munka nagy részét három fiatal kutató – Garai Ágnes, Zeke András és Gógl Gergő – végezte. A 2008 óta ezen a néven hetente megjelenő Science Signaling jelátviteli kutatásokkal foglalkozik, a Science tudományos magazin „leánylapja”.